Anemia - jeden z objawów celiakii


Autor: Jabłońska Klaudia dietetyk kliniczny
Niedokrwistość (anemia) jest stanem, w którym we krwi występuje zbyt mała ilość czerwonych krwinek lub gdy w ich wnętrzu jest mało hemoglobiny, która transportuje tlen. Do produkcji czerwonych krwinek niezbędne jest żelazo, kwas foliowy i witamina B12.
Niedokrwistość pojawia się, gdy nasze zasoby żelaza w organizmie są wyczerpane, a organizm nie uzupełnił ich ze źródeł pokarmowych. Taka sytuacja doprowadza do obniżenia stężenia hemoglobiny, co skutkuje niedotlenieniem i zmniejszeniem czerwonych krwinek, doprowadzając do osłabienia i przewlekłego zmęczenia.
Jakie mogą być przyczyny anemii u pacjentów z celiakią?
Niedokrwistość z niedoboru żelaza jest częstym objawem w celiakii, występuje u 40% pacjentów. Dwie główne przyczyny to zanik kosmków błony śluzowej w miejscu wchłaniania żelaza (dwunastnica) i wynikający z tego stan zapalny, który uruchamia mechanizm prowadzący do niedokrwistości choroby przewlekłej.
Co więcej, niektórzy pacjenci z celiakią są oporni na doustną suplementację żelazem pomimo gojenia błony śluzowej, a zatem wymagają okresowego dożylnego podawania żelaza. Nawet w przypadku nadwrażliwości na gluten bez celiakii, niedokrwistość występuje u 18,5–22% pacjentów i wydaje się być związana z ultrastrukturalnymi i molekularnymi zmianami w mikrokosmkach jelitowych.
Celiakia jest globalnym problemem zdrowotnym, ponieważ jej częstość występowania potwierdzone biopsją szacuje się na ponad 1% populacji w świecie zachodnim i zachorowalność na nią stale rośnie. Jest ona najwyższa u kobiet i dzieci, a niedokrwistość jest jednym z najczęstszych objawów klinicznych celiakii i może występować u ponad połowy pacjentów w momencie rozpoznania. Przewlekły stan zapalny może również odgrywać rolę w rozwoju anemii w celiakii.
Mechanizm wchłaniania żelaza w normalnych warunkach
Żelazo jest niezbędnym mikroelementem dla wszystkich komórek, ponieważ jest potrzebne do erytropoezy, metabolizmu oksydacyjnego i aktywności enzymatycznej, a także jest kofaktorem enzymów mitochondrialnego łańcucha oddechowego, cyklu kwasu cytrynowego i syntezy DNA. Promuje również wzrost komórek układu odpornościowego.
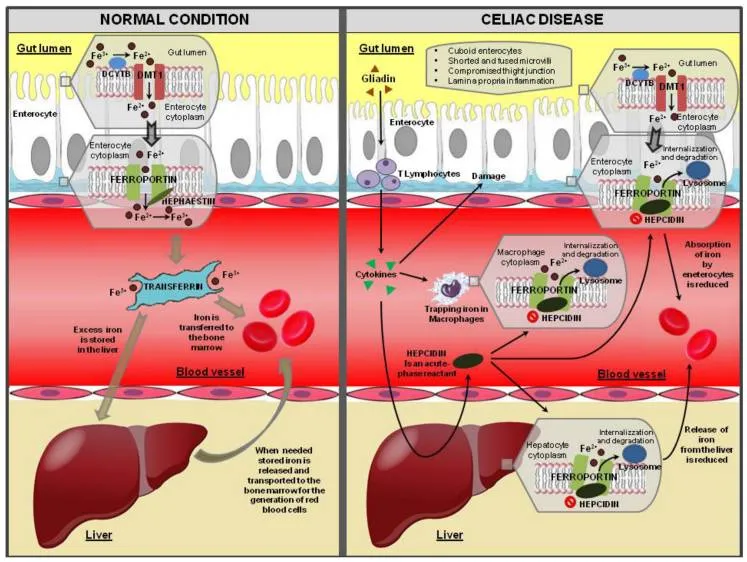
Żelazo niehemowe występuje w diecie głównie w postaci żelaza (Fe 3+ ). Wchłaniane żelazo musi zostać przekształcone z formy Fe 3+ w formę żelaza (Fe 2+ ) na błonie wierzchołkowej enterocytów dwunastnicy lub w diecie środkiem redukującym może być kwas askorbinowy. Żelazo w postaci Fe 2+ jest następnie transportowane przez błonę wierzchołkową dwunastnicy przez symporter żelaza, transporter metali dwuwartościowych 1 (DMT1). DMT1 jest białkiem znajdującym się na błonie rąbka szczoteczkowego i może przenosić żelazo i wiele innych metali dwuwartościowych . Jest więc przechowywany wewnątrz enterocytów. Fe2 + jest następnie przenoszony do krwi za pośrednictwem eksportera żelaza, ferroportyny. W celu transportu w krwiobiegu żelazo wiąże się z transferyną, która może transportować dwa jony żelaza (Fe 3+ ) do odległych tkanek docelowych. Przed wiązaniem transferyny jony żelazawe (Fe 2+ ) muszą zostać ponownie przekształcone w jony żelazowe (Fe 3+ ). Nadmiar żelaza może odkładać się w wątrobie, a następnie może zostać uwolniony i wykorzystany później. Homeostazę żelaza reguluje hepcydyna, hormon syntetyzowany przez hepatocyty i wydzielany do krwi. Poprzez internalizację i degradację ferroportyny, hepcydyna zmniejsza dopływ żelaza do osocza krwi z dwunastnicy, z makrofagów biorących udział w recyklingu starzejących się erytrocytów oraz z hepatocytów.
Doniesiono, że cytokiny prozapalne — w szczególności interferon gamma (IFN-y), interleukina-6 (IL-6) i czynnik martwicy nowotworu-α (TNF-α) – wyzwalają syntezę hormonu regulującego żelazo , hepcydyna, która powoduje rozkład ferroportyny i hamuje uwalnianie żelaza przez makrofagi i enterocyty.
A więc co powoduje brak wchłania żelaza w celiakii?
W normalnych warunkach żelazo jest wchłaniane w przewodzie pokarmowym, a następnie dostarczane do transferyny w celu transportu do rozwijających się krwinek czerwonych, nadmiar żelaza jest magazynowany w hepatocytach. W celiakii, z powodu zaniku kosmków w błonie śluzowej jelit, dochodzi do zmniejszonego wchłaniania żelaza w jelitach, a tym samym do zmniejszonego dostarczania żelaza do rozwijających się krwinek czerwonych. Ponadto, współistniejące zapalenie błony śluzowej wywołane przez gluten powoduje zwiększone uwalnianie cytokin, co może indukować zwiększoną produkcję hepcydyny w wątrobie, która hamuje ferroportynę (główne białko eksportujące żelazo) i w konsekwencji zmniejsza uwalnianie żelaza z enterocytów, hepatocytów i krążących makrofagów.
Żelazo jest specyficznie wchłaniane w dwunastnicy, która jest miejscem poważnego stanu zapalnego i urazu u pacjentów z celiakią, ten mechanizm wyjaśnia, dlaczego niedokrwistość z niedoboru żelaza jest główną postacią anemii w celiakii.
Może również wystąpić złe wchłanianie kwasu foliowego i witaminy B12 , ale najczęściej występuje u pacjentów z celiakią z bardziej rozległymi zmianami. Połączenie niedoboru żelaza i kwasu foliowego, witaminy B12 może powodować specyficzne zmiany morfologiczne krwinek czerwonych.
Jakie mogą być jeszcze przyczyny niedokrwistości z niedoboru żelaza w celiakii?
Innymi przyczynami niedokrwistości z niedoboru żelaza u pacjentów z celiakią mogą być :
-
inne choroby zapalne jelit (np. nieswoiste zapalenia jelit i lamblioza),
-
choroby pozajelitowe (np. zapalenie stawów i zapalenia skóry),
-
utraty krwi utajonej w przewodzie pokarmowym (np. współistniejące pasożyty jelitowe, enteropatie polekowe, neoplazja jelit i infekcja żołądka przez Helicobacter pylori ),
-
zwiększone zapotrzebowanie na żelazo (np. w czasie ciąży i podczas uprawiania sportów wyczynowych).
-
u pacjentów z celiakią niedokrwistość może powodować nieodpowiednia dieta uboga w żelazo, ponieważ dieta bezglutenowa nie jest wzbogacana żelazem jak żywność z pszenicy.
Przewlekłe zapalenie jelit
Stanom zapalnym często towarzyszy niedokrwistość mikrocytarna, która może prowadzić do zmiany homeostazy żelaza. Po pierwsze, cytokiny zapalne hamują produkcję erytropoetyny w nerkach. Po drugie, dostępność żelaza jest zmniejszona dzięki hepcydynie, która jest reagentem ostrej fazy. Hepcydyna, która wiąże i obniża poziom ferroportyny, zapobiega przenoszeniu żelaza z enterocytów i zapasów organizmu do krwi w celu wytwarzania czerwonych krwinek. Podwyższone poziomy białek ostrej fazy w surowicy, takich jak białko C-reaktywne (CRP), są rzadkie w celiakii, chociaż aktywacja komórek jednojądrzastych blaszki właściwej błony śluzowej , zależna od gliadyny, powoduje nadprodukcję cytokin prozapalnych, takich jak IFN-γ i IL-6, które są mediatorami anemii i ogólnoustrojowego zapalenia . W celiakii IFN-γ jest główną cytokiną wydzielaną przez komórki zapalne błony śluzowej jelita po ekspozycji na gluten. IFN-γ, TNF-α, IL-1, IL-6, IL-15 i IL-33 są podwyższone w celiakii i są uważane za oznaki aktywnej choroby. IL-6 i IFN-y hamują ekspresję mRNA receptora transferyny, a IFN-y sprzyja retencji żelaza w monocytach i hamuje erytropoezę poprzez IL-15. IL-15 bierze udział w patofizjologii zapalenia w celiakii i jest częściowo odpowiedzialna za przedłużający się stan zapalny. Cytokiny te są uwalniane do krążenia i działają na wątrobę, powodując indukcję hepcydyny, której rolą jest hamowanie wchłaniania żelaza z dwunastnicy. Cytokiny te również zwiększają poziom DMT-1 obecnego na makrofagach, zwiększając w ten sposób ich wchłanianie żelaza, ale jednocześnie zmniejszają poziom ferroportyny (która jest transbłonowym eksporterem żelaza). Mechanizmy te zapobiegają uwalnianiu żelaza z makrofagów do krążenia, a efektem jest uwięzienie żelaza w układzie siateczkowo-śródbłonkowym. To sugeruje, że wywołane glutenem reakcje zapalne w błonie śluzowej jelit mogą odgrywać główną rolę w określaniu złego wchłaniania żelaza, rozregulowaniu homeostazy żelaza i nieskutecznej produkcji erytropoetyny, prowadząc w ten sposób do anemii u niektórych pacjentów. Poprawa stanu zapalnego i atrofii błony śluzowej jelit, którą można uzyskać za pomocą diety bezglutenowej, może prowadzić do postępującej korekcji anemii, zarówno poprzez poprawę wchłaniania żelaza, jak i zmniejszenie wpływu różnych mediatorów stanu zapalnego na homeostazę żelaza i erytropoezę.
Jak leczyć anemię z niedoboru żelaza u pacjentów z celiakią?
Podstawą leczeni pacjentów z celiakia jest dieta bezglutenowa, która dość szybko daje efekt ustąpienia objawów klinicznych, natomiast zmiany histologiczne ustępują po około 8 tygodniach. Ścisłe przestrzeganie diety bezglutenowej i dbanie o zwiększoną podaż żelaza w diecie pozwoli wyrównać niedobory w organizmie. Należy pamiętać o stosowaniu diety przeciwzapalnej i o związkach, które spowalniają wchłanianie żelaza ( fityniany - obecne w orzechach, kaszach , grochu i taninach - obecny w herbacie, kawie i kakao).
Żywność bogata w żelazo to rośliny strączkowe, mięso wołowe i wieprzowe, jagnięcina, drób , żółtka jaj , natka pietruszki , szpinak , pestki dyni, morele, siemię lniane.
Jeśli chcesz więcej dowiedzieć się na temat celiakii zapraszam do artykułu celiakia "choroba na całe życie"
Bibliografia:
-
Ludvigsson J.F., Bai J.C., Biagi F., Card T.R., Ciacci C., Ciclitira P.J., Green P.H.R., Hadjivassiliou M., Holdoway A., van Heel D.A., et al. Diagnosis and management of adult coeliac disease: Guidelines from the British Society of Gastroenterology. Gut. 2014
-
King J.A., Jeong J., Underwood F.E., Quan J., Panaccione N., Windsor J.W., Coward S., deBruyn J., Ronksley P.E., Shaheen A.-A., et al. Incidence of Celiac Disease Is Increasing Over Time: A Systematic Review and Meta-analysis. Am. J. Gastroenterol. 2020
-
Halfdanarson T.R., Litzow M.R., Murray J.A. Hematologic manifestations of celiac disease. Blood. 2007;
-
Martín-Masot R., Nestares M.T., Diaz-Castro J., López-Aliaga I., Alférez M.J.M., Moreno-Fernandez J., Maldonado J. Multifactorial Etiology of Anemia in Celiac Disease and Effect of Gluten-Free Diet: A Comprehensive Review. Nutrients. 2019;
-
Freeman H.J. Iron deficiency anemia in celiac disease. World J. Gastroenterol. 2015
-
Weiss G., Goodnough L.T. Anemia of chronic disease. N. Engl. J. Med. 2005
-
Hershko C., Patz J. Ironing out the mechanism of anemia in celiac disease. Haematologica. 2008
-
Nemeth E., Rivera S., Gabayan V., Keller C., Taudorf S., Pedersen B.K., Ganz T. IL-6 mediates hypoferremia of inflammation by inducing the synthesis of the iron regulatory hormone hepcidin. J. Clin. Investig. 2004
-
Annibale B., Severi C., Chistolini A., Antonelli G., Lahner E., Marcheggiano A., Iannoni C., Monarca B., Delle Fave G. Efficacy of gluten-free diet alone on recovery from iron deficiency anemia in adult celiac patients. Am. J. Gastroenterol. 2001
-
Illing A.C., Shawki A., Cunningham C.L., Mackenzie B. Substrate profile and metal-ion selectivity of human divalent metal-ion transporter-1. J. Biol. Chem. 2012
-
DeLoughery T.G. Microcytic anemia. N. Engl. J. Med. 2014
-
Weiss G., Gasche C. Pathogenesis and treatment of anemia in inflammatory bowel disease. Haematologica. 2010
